Група от независими съветници към Администрацията по храните и лекарствата на САЩ (FDA) гласува против одобрението на имплант с GLP-1 агонист за лечение на диабет, съобщиха от американския лекарствен регулатор. Мотивите на експертите са рискове от потенциални странични ефекти, засягащи основно бъбреците и сърдечносъдовата система.
Според съветниците, които са взели решението си единодушно, ползите от комбинацията лекарство плюс устройство за лечение на диабет тип 2 не надвишават рисковете и е необходимо да се представят допълнителни данни за безопасност.
Решението идва след две предшестващи отхвърляния от страна на здравния регулатор поради потенциално остро бъбречно увреждане и увеличени сърдечносъдови рискове на лекарството.
В заключенията на експертите фигурира и информация за дисбаланс в броя на възникналите проблеми с остро бъбречно увреждане в групата, провеждала лечение с импланта, спрямо групата на плацебо.
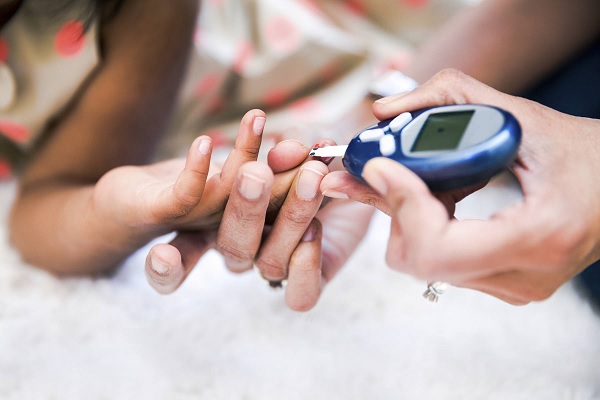
Кандидатът за лекарствено устройство с размер на кибритена клечка, наречен ITCA 650, използва помпа, която може да се имплантира под кожата при пациенти с диабет тип 2, за да достави лекарството екзенатид – GLP-1 агонист за продължителен период – до една година.
Робърт Гриви, един от съветниците в групата на FDA, смята, че принципно това е една добра перспектива за пациентите с диабет тип 2, но представените данни са недостатъчни, за да бъдат в регулатора убедени, че това е най-добрата версия на устройството.
Екзенатид принадлежи към придобилите напоследък огромна популярност GLP-1 рецепторни агонисти, предназначени за контрол на кръвната захар при диабетици, а така също и за потискане на апетита и засилване на чувството за ситост.